研究背景
急性髓系白血病(AML)的免疫治疗长期受困于肿瘤微环境的免疫抑制状态。虽然mRNA疫苗能够编码肿瘤抗原,但抗原呈递细胞功能失常、T细胞耗竭等问题严重限制了疗效。如何在树突状细胞中同时实现mRNA抗原表达与STAT3免疫检查点的沉默,成为逆转免疫抑制的核心挑战。
助力研究
2025年,中国药科大学尹莉芳团队联合上海高等研究院李娜团队在《Journal of the American Chemical Society》(JACS)发表研究论文。团队开发了一系列具有“M型”极性头构象和多隔室内部结构的咪唑基脂质纳米颗粒(A3-DM/DL-LNPs),实现了mRNA与siSTAT3的高效共递送,并在动物模型中成功恢复了树突状细胞功能、缓解内质网应激、逆转T细胞耗竭,显著增强了抗白血病免疫应答。
在该研究中,艾锐 Polar-SIM 超分辨成像系统为揭示LNP的胞内命运提供了最核心的可视化依据。

Polar-SIM 在该文中的贡献
活细胞超分辨成像:直观区分高效递送与溶酶体陷阱
纳米颗粒能否实现RNA药物的胞质递送,关键在于能否避免被溶酶体捕获并完成快速逃逸。研究团队利用 Polar-SIM 的高时空分辨率与低光毒性成像能力,对DC2.4活细胞中不同LNP制剂的胞内转运过程进行了长达5分钟的动态追踪。
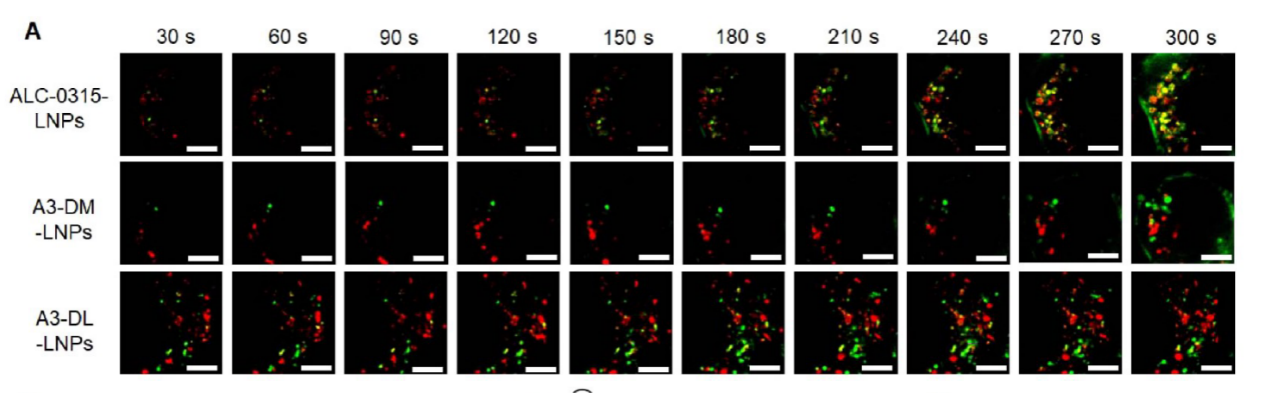
Figure 4A. Representative images showing cellular uptake of FITC-labeled ALC-0315-LNPs, A3-DM-LNPs, and A3-DL-LNPs in DC 2.4 cells, acquiring images every 30 s using a Polar-SIM High-fidelity Polarized Super-Resolution Microscopy. Lysosomes were stained with LysoTracker Red. Scale bar is 5 μm.
Figure 4A. 显示FITC标记的ALC-0315-LNPs、A3-DM-LNPs和A3-DL-LNPs在DC 2.4细胞中获取的代表性图像,使用 Polar-SIM 高保真偏振超分辨率显微镜每30秒采集一幅图像。溶酶体用LysoTracker Red染色。比例尺为5 μm。
临床级ALC-0315-LNPs呈现密集的黄色荧光,与溶酶体高度重叠,大量被困于溶酶体网络中。
而A3-DM-LNPs和A3-DL-LNPs则在胞质中显示出强烈的绿色荧光,与溶酶体的共定位极低,直观证明了它们具备更高效的溶酶体逃逸能力。
定量分析进一步证实,ALC-0315-LNPs与溶酶体的皮尔逊共定位系数高达0.72,而A3-DM-LNPs和A3-DL-LNPs分别仅为0.17和0.36。这一数据为“M型”脂质构象能够重塑LNP胞内转运路径、绕过溶酶体降解提供了直接证据。
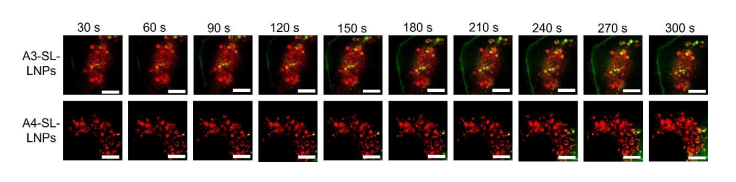
Figure S26. Uptake efficiency of FITC-labeled A3-SL-LNPs and A4-SL-LNPs in DC2.4 cells, assessed by Polar-SIM High-fidelity Polarized Super-Resolution Microscopy. Lysosomes were selectively stained using Lyso Tracker Red. Scale bar, 5 μm.
Figure S26. FITC标记的A3-SL-LNPs和A4-SL-LNPs在体内的摄取效率 DC2.4细胞,用 Polar-SIM 高保真极化超分辨显微镜。溶酶体用Lyso Tracker Red染色。比例尺为5 μm。

总结
本研究通过结构-活性关系的系统优化,成功构建了能够同时递送mRNA和siSTAT3的多隔室LNP平台,为克服AML免疫治疗耐受提供了全新策略。
艾锐 Polar-SIM 超分辨成像系统在本研究中发挥了不可替代的作用。其在活细胞水平上兼具高分辨率与低光毒性的独特优势,使研究团队能够首次清晰捕捉到不同LNP制剂与溶酶体的动态相互作用过程,为“M型”构象介导的溶酶体逃逸机制提供了最直观的验证,成为连接脂质分子设计与生物学功能的关键桥梁。
原文链接:
https://pubs.acs.org/doi/10.1021/jacs.5c23209




 公安备案号:京公网安备11010802046288号
公安备案号:京公网安备11010802046288号